Maximální OBJEMOVÁ STABILITA
NEJČISTĚJŠÍ objemově stabilní bovinní kost
cerabone® byl úspěšně použit u více než 1 milionu pacientů v regenerační stomatologii a používá se již více než 15 let v různých lékařských aplikacích (např. kraniofaciální chirurgie, onkologie a chirurgie rukou a páteře).
JEDINEČNÝ
VÝROBNÍ PROCES
cerabone® se vyrábí z vybrané stehenní kosti skotu jedinečným
výrobním procesem
o teplotě 1200 °C, který využívá pouze teplo a vodu (bez chemických přísad).
100% ČISTÝ
KOSTNÍ MATERIÁL
Unikátní proces
zpracování odstraní všechny organické složky, což má za následek
kostní minerál s výjimečnou čistotou 1 .
PORÉZNÍ A
BIOAKTIVNÍ POVRCH
Struktura kosti cerabone® je díky její trojrozměrné porézní síti a bioaktivnímu povrchu
podobná lidské kosti. Podporuje adhezi a invazi buněk a formování nové kosti, což zajišťuje úplnou integraci do nově vytvořené kostní matrix 2 .
VYNIKAJÍCÍ
HYDROFILITA
propojené trojrozměrné póry a hrubý, extrémně hydrofilní povrch cerabone® podporuje adhezi proteinů z krve 3 .
DEPOT
EFEKT
100% čistý přírodní kostní minerál působí jako
rezervoár vápníku, který pomalu uvolňuje ionty vápníku pro remodelaci kostí 4 . Drsný povrch nepřetržitě váže a uvolňuje signální molekuly, což zajišťuje
dlouhodobý depotní účinek.
DLUHODOBÝ
KLINICKÝ VÝSLEDEK
Retrospektivní analýzy* prokázaly dlouhodobou stabilitu cerabone® s kumulativní uspěšností u zavedeného implantátu 98.73 – 100% 5-9 .
*with mean follow-ups of 12 – 65.93 months and dental implants placed in solely cerabone®-grafted sites or sites augmented with cerabone® in combination with autologous bone
100% ČISTÝ KOSTNÍ MATERIÁL
Dlouhodobý úspěch bovinní kosti cerabone® je založen na vynikajících osteokonduktivních vlastnostech a vynikající čistotě materiálu dosažené jedinečným 1200°C tepelným zpracováním.
cerabone® se vyrábí z vybrané stehenní kosti skotu jedinečným zpracováním za vysokých teplot bez chemických přísad pouze za použití tepla a vody. Tímto sofistikovaným zpracováním se vytvoří kostní minerál s výjimečnou čistotou a vysokým stupněm krystalinity. Na rozdíl od neslinutých bovinních kostních štěpů nejsou přítomny žádné zbytky vody a uhličitanu vápenatého 1 .
Struktura bovinní kosti cerabone® je podobná lidské kosti
Díky své trojrozměrné síťové porozitě a drsnému povrchu podporuje cerabone® tvorbu krevní sraženiny a rychlý a efektivní průnik tekutinami, krví a bílkovinami, což dokazují jeho vynikající hydrofilní vlastnosti. Signální molekuly z krve jsou vázány a postupně uvolňovány z částic, čímž cerabone® poskytuje dlouhodobý depotní účinek. Vysoká krystalinita zajišťuje kontrolované a pomalé uvolňování iontů vápníku do okolní tkáně. Cerabone® tedy působí také jako rezervoár vápníku důležitý pro přestavbu kosti.
Jak vysoký stupeň krystalinity, tak fázová čistota poskytují maximální objemovou stabilitu.
Histomorfometrická analýza lidských biopsií hodnotících resorpci cerabonu® našla jen minimální informace o degradaci materiálu, jako jsou fagocytované částice biomateriálu 10 . Po aplikaci jsou částice cerabonu® resorbovány pouze povrchově a lze je i po letech v oblasti augmentace najít, což poskytne trvalou strukturální podporu.
Buněčná kostní integrace
Po aplikaci se různé typy buněk zapojených do kaskády hojení ran a růstové faktory pocházející z oblasti rány vážou na povrch granulí cerabone®. Následně se prekurzorové buňky diferencují na osteoblasty a začnou produkovat novou kostní matrici. Po několika měsících (6-9 měsících) jsou částice cerabonu® integrovány do nově vytvořené kostní matrice a povrch je zcela pokryt novou mineralizovanou kostí, což vede k dlouhodobě stabilní situaci kosti 11
Míra přežití implantátu 98,73 – 100%
Zubní implantáty implantované pomocí augmentace cerabone®, nebo implantovaná místa augmentovaná cerabone® v kombinaci s autologní kostí, prokázaly dlouhodobou stabilitu s kumulativní mírou přežití implantátu 98,73 – 100%, průměrná doba sledování 12 – 65,93 měsíce po operaci 5-9 .
cerabone® PRODUKTOVÁ ŘADA
cerabone® je k dispozici ve formě granulí nebo bloku.
cerabone® granule se dodávají ve dvou velikostech a v osmi různých objemech: malé granule (0.5 – 1.0 mm) a velké granule (1.0 – 2.0 mm).
cerabone® blok je k dispozici ve velikosti 20 x 20 x 10 mm.
MALÉ GRANULE
Malé granule cerabone® jsou zvláště vhodné pro konturování kosti, např. pro augmentaci estetické oblasti, nebo k vyplnění zbývajících mezer v kosti při provádění augmentace pomocí kostního bloku. Malé granule se také přednostně používají k regeneraci menších defektů a intraoseálních defektů.
VELKÉ GRANULE
Velké granule cerabone® jsou vhodné především pro augmentaci velkoobjemových defektů (např. sinus lift). Kromě většího objemu který velké granule mají, je mezi velkými granulemi také více prostoru, což umožňuje lepší revaskularizaci větších defektů.
cerabone® MALÉ granule
| Velikost částic | Obsah | |
|---|---|---|
| 1520 | 1.0 – 2.0 mm | 1 × 0.5 ml |
| 1521 | 1.0 – 2.0 mm | 1 × 1.0 ml |
| 1522 | 1.0 – 2.0 mm | 1 × 2.0 ml |
| 1525 | 1.0 – 2.0 mm | 1 × 5.0 ml |
cerabone® VELKÉ granule
| Č. Výr. | Velikost částic | Obsah |
|---|---|---|
| 1520 | 1.0 – 2.0 mm | 1 × 0.5 ml |
| 1521 | 1.0 – 2.0 mm | 1 × 1.0 ml |
| 1522 | 1.0 – 2.0 mm | 1 × 2.0 ml |
| 1525 | 1.0 – 2.0 mm | 1 × 5.0 ml |
cerabone® blok
| Č. Výr. | Dimenze | Obsah |
|---|---|---|
| 1720 | 20×20×10 mm | 1 × blok |

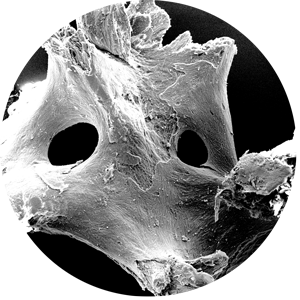
POROZITA & BIOAKTIVNÍ POVRCH
Geometrie a topografie jsou rozhodující pro to, aby byl materiál pro augmentaci kostí integrován a / nebo resorbován během procesu přirozeného hojení těla. Aby se po implantaci kostní náhrady vytvořila nová kostní matrice, musí se regenerační buňky usadit, proliferovat a diferencovat. Během těchto událostí je nezbytný jejich neustálý přísun živin, což vyžaduje tvorbu a šíření krevních cév v kostním štěpu.
Propojená pórovitost a póry různých velikostí poskytují prostor pro angiogenezi a depozici kostní matrice, zatímco strukturovaná povrchová morfologie umožňuje adhezi pluripotentních buněk, které jsou výchozím bodem pro regeneraci kostí.
cerabone® svými jedinečnými vlastnostmi materiálu poskytuje toto prostředí přátelské k buňkám a účinně tak podporuje kostní regenerační proces. cerabone® je vysoce porézní kostní augmentační materiál s porozitou ~ 65-80% a střední velikostí pórů ~ 600-900 um 12 . Makropóry umožňují rychlý růst krevních cév a buněk tvořících kosti, zatímco mikropóry podporují rychlý příjem krve kapilárním účinkem.
Elektronové mikroskopické obrázky (SEM) demonstrují vysoce strukturovaný povrch cerabonu®. Usnadňuje adhezi signálních proteinů a buněk z krve. Adherující osteoblasty mohou iniciovat tvorbu kostní matrice, což vede k kostní integraci částic.
VYNIKAJÍCÍ HYDROFILITA
Krev účinně pronikající do částic je nezbytná pro kostní integraci materiálu pro úspěšnou augmentaci kosti, protože poskytuje všechny biologické informace nezbytné pro hojení ran a tvorbu nové kosti.
Například poskytuje kmenové buňky schopné diferenciace na osteogenní buňky tvořící novou kostní tkáň. Signální molekuly rozpuštěné v krevní plazmě organizují pro- a protizánětlivé procesy probíhající po implantaci biomateriálu. Souhra obou procesů je považována za zásadní pro dlouhodobou stabilní integraci a / nebo resorpci kostního náhradního materiálu.
Drsný povrch a vzájemně propojené póry cerabonu® poskytují optimální podmínky pro všechny důležité složky krve. Vede k vynikající hydrofilitě, která se ukázala být lepší ve srovnání s jinými materiály pro augmentaci kostí 3 . Silný kapilární účinek umožňuje rychlý a efektivní průnik tekutin, krve a proteinů do trojrozměrné trabekulární sítě částic, čímž podporuje jejich kostní integraci.
Kromě toho vynikající hydrofilní vlastnosti cerabone® umožňují pohodlnou manipulaci s částicemi, protože po hydrataci dobře drží pohromadě.
DEPOT EFEKT
cerabone® poskytuje biologický a minerální depot, který podporuje kostní regenerační proces.
Biologický depotní účinek je dán hostitelskými proteiny a živinami, které mají interakci s částicemi cerabonu®. Předklinické analýzy prokázaly, že signální molekuly z krve jsou vázány a postupně uvolňovány z částic, čímž poskytuje cerabone® dlouhodobý depotní účinek 13 . Cytokiny a další chemotaktické proteiny jsou tedy dodávány do místa augmentace, které získávají kmenové buňky pro diferenciaci na osteoblasty a buňky vrozeného imunitního systému zapojené do časného hojení ran.
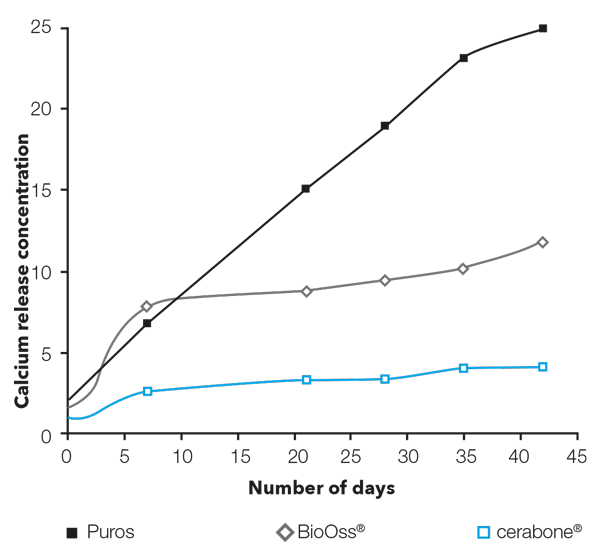
Minerální depotní účinek se připisuje hlavně vápníku a je zajištěn jedinečným chemickým složením cerabone®. Během růstu kosti a jejího přechodu do mechanicky silné lamelární kosti vyžaduje proces mineralizace značné množství minerálů, jako jsou ionty vápníku. Jakmile jsou kolagenové fibrily a další organické složky vylučovány a ukládány osteoblasty, minerály se vysráží. Vysoká krystalinita cerabone® podporuje mineralizaci formující se kosti, protože zajišťuje kontrolované a pomalé uvolňování vápníku do okolní tkáně, takže cerabone® působí jako stálý rezervoár vápníku důležitý pro proces remodelace kosti 14.
Uvolňování vápníku stanoveno atomovou absorpční spektroskopií 4
Integrace cerabonu ® do nově vytvořené kostní matrice je výsledkem komplexních biologických událostí, které probíhají po implantaci.
Unikátní topografické a fyzikálně-chemické vlastnosti cerabonu ® účinně podporují tvorbu krevních sraženin a množení regeneračních buněk, což vede k předvídatelné integraci částic. Jeho neresorbovatelnost díky své výjimečné čistotě dlouhodobě zajišťuje stabilitu augmentované kosti.
> 1 MILION
LÉČENÝCH PACIENTŮ
> 15 LET KLINICKÝCH ZKUŠENOSTÍ
V DALŠÍCH LÉKAŘSKÝCH OBORECH
V >100 ZEMÍCH
> 150 VĚDECKÝCH
PŘÍSPĚVKŮ A STUDIÍ
LITERATURA
1 Tadic, D. and Epple, M. (2004), “A thorough physicochemical characterisation of 14 calcium phosphate-based bone substitution materials in comparison to natural bone”, Biomaterials, Vol. 25 No. 6, pp. 987–994.
2 Rothamel D, Schwarz F, Smeets R, Happe A, Fienitz T, Mazor Z, Zöller J. Sinus floor elevation using a sintered, natural bone mineral zzi 27(1) 2011
3 Trajkovski B., Jaunic, M., Müller W.H., Beuer F., Zafiropoulos G.-G. and Houshmand A. Hydrophilicity, Viscoelastic, and Physico chemical Properties Variations in Dental Bone Grafting Substitutes. Materials 2018, 11(2), 215.
4 Berberi A, Samarani A, Nader N, Noujeim Z, Dagher M, Kanj W, Rita Mearawi,1 Ziad Salemeh,1 and Bassam Badran2 Physicochemical characteristics of bone substitutes used in oral surgery in comparison to autogenous bone. Biomed Res Int. 2014;2014:320790.
5 Tawil G, Tawil P, Khairallah A. Sinus Floor Elevation Using the Lateral Approach and Bone Window RepositioningI: Clinical and Radiographic Results in 102 Consecutively Treated Patients Followed from 1 to 5 Years. Int J Oral Maxillofac Implants. 2016 Jul-Aug;31(4):827-34.
6 Cardaropoli D, Tamagnone L, Roffredo A, De Maria A, Gaveglio L. Preservation of Peri-implant Soft Tissues Following Immediate Postextraction Implant Placement. Part II: Clinical Evaluation. Int J Periodontics Restorative Dent. 2019 Nov/Dec;39(6):789-797.
7 Kamadjaja DB, Sumarta NPM, Rizqiawan A. Stability of Tissue Augmented with Deproteinized Bovine Bone Mineral Particles Associated with Implant Placement in Anterior Maxilla. Case Rep Dent. 2019 Oct 27;2019:5431752.
8 Lorean A, Mazor Z, Barbu H, Mijiritsky E, Levin L. Nasal floor elevation combined with dental implant placement: a long-term report of up to 86 months. Int J Oral Maxillofac Implants. 2014 May-Jun;29(3):705-8.
9 Khojasteh A, Hassani A, Motamedian SR, Saadat S, Alikhasi M. Cortical Bone Augmentation Versus Nerve Lateralization for Treatment of Atrophic Posterior Mandible: A Retrospective Study and Review of Literature. Clin Implant Dent Relat Res. 2016 Apr;18(2):342-59.
10 Barbeck M, Udeabor S, Lorenz J, Schlee M, Holthaus MG, Raetscho N, Choukroun J, Sader R, Kirkpatrick CJ, Ghanaati S.High-Temperature Sintering of Xenogeneic Bone Substitutes Leads to Increased Multinucleated Giant Cell Formation: In Vivo and Preliminary Clinical Results. J Oral Implantol. 2015;41(5):e212-22.
11 Tawil G, Barbeck M, Unger R, Tawil P, Witte F. Sinus Floor Elevation Using the Lateral Approach and Window Repositioning and a Xenogeneic Bone Substitute as a Grafting Material: A Histologic, Histomorphometric, and Radiographic Analysis. Int J Oral Maxillofac Implants. 2018 September/October;33(5):1089–1096.
12 Seidel P, Dingeldein E. cerabone® – Bovine Based Spongiosa Ceramic Seidel et al. Mat.-wiss. u. Werkstofftech. 2004
13 In vitro experiments from Prof. Dr. H. Jennissen and Dr. M. Laub University of Duisburg-Essen/Morphoplant GmbH
14 Riachi F, Naaman N, Tabarani C, Aboelsaad N, Aboushelib MN, Berberi A, Salameh Z. Influence of material properties on rate of resorption of two bone graft materials after sinus lift using radiographic assessment. Int J Dent. 2012;2012:737262.
